- تماس با ما
- 09121001976
- parspalma@gmail.com

باتری و اسباب بازی
۱۳۹۷-۰۷-۲۱
تاریخچه باتری قسمت ۱
۱۳۹۷-۰۷-۲۱باتری چیست ؟
معرفی:
باتری ها مجموعه ای از یک یا چند سلول هستند که واکنش های شیمیایی جریان الکترون ها را در یک مدار ایجاد می کنند و اما باتری چیست ؟
تمام باتری ها از سه جزء اساسی ساخته شده اند:
یک آند(سمت – ) ، یک کاتد (سمت+) و بعضی انواع الکترولیت (ماده ای که بطور شیمیایی با آند و کاتد واکنش می دهد).
هنگامی که آند و کاتد باتری به یک مدار متصل می شوند،واکنش شیمیایی بین الکترولیت اتفاق می افتد.
این واکنش باعث می شود که الکترون ها از طریق مدار جریان یابند و به کاتد که در آن واکنش شیمیایی دیگر اتفاق می افتد.
هنگامی که مواد در کاتد یا آند مصرف می شوند یا دیگر قادر به استفاده در واکنش نیستند، باتری دیگر قادر به تولید برق نیست.
در آن لحظه باتری شما “مرده” است.باتری هایی که می توانند دوباره شارژ شوند،باتری های ثانویه نامیده می شوند.
برای مثال، باتری های لیتیوم پلیمر می توانند دوباره شارژ شوند.
بدون باتری quadcopter شما باید به دیوار وصل شود،باید به ماشین خود لگد بزنید و کنترل کننده ی xbox شما باید تمام وقت (مثل روزهای خوب قدیمی) وصل باشد.
باتری ها راهی برای ذخیره انرژی پتانسیل الکتریکی در یک ظرف قابل حمل ارایه می دهند.
اختراع باتری مدرن اغلب به الساندرو ولتا نسبت داده می شود.
این در واقع با یک حادثه شگفت آور در ارتباط با تشریح قورباغه آغاز شد.
تاریخچه:
اصطلاح باتری چیست
از نظر تاریخی باتری چیست ؟ کلمه “باتری” برای توصیف “مجموعه ای از اشیا مشابه که برای انجام یک کار باهم دسته بندی شدند” استفاده می شد ؛
مانند یک باتری توپخانه.
در سال ۱۷۴۹ ، بنجامین فرانکلین برای اولین بار از این اصطلاح برای توصیف یک سری از خازن هایی که برای آزمایش الکتریکی خود بهم مرتبط کرده بود ، استفاده کرد.
بعد ها این اصطلاح برای هر سلول الکتروشیمیایی که برای هدف تامین نیروی برق بهم مرتبط می شدند ، استفاده می شد
بهترین پخش عمده باتری را از کجا پیدا کنیم؟
اختراع باتری چیست
در سال ۱۷۸۰ ، فیزیکدان ، پزشک ، زیست شناس ، و فیلسوف ایتالیایی “لوگی گالوانی” یک قورباغه را که به قلاب برنجی ای متصل بود را تشریح می کرد.
هنگامیه که پای قورباغه را با یک تیغ جراحی فلزی لمس کرد ، پا تکانی ناگهانی خورد.گالوانی نظریه داد که آن انرژی از خود پا آمده اما همکار دانشمندش “الساندرو وولتا” عقیده دیگری داشت.
وولتا فرض کرد که تکان ناگهانی پای قورباغه در حقیقت ناشی از فلزات خیس در مایع بوده است.
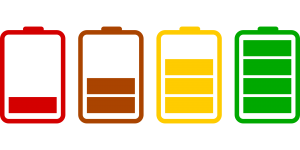
او آزمایش را بجای جسد قورباغه ، با استفاده از لباس خیس شده در آب نمک تکرار کرد که منجر به ولتاژی مشابه شد.وولتا یافته های خود را در سال ۱۷۹۱ منتشر کرد و سپس اولین باتری “پیل وولتا” را در سال ۱۸۰۰ ساخت.
پیل وولتا گرفتار دو مشکل اساسی شد:
وزن توده باعث شد که الکترولیت از پارچه خارج شود و خواص شیمیایی خاص اجزا در مدت بسیار کوتاهی نتیجه داد (حدود یک ساعت). دویست سال بعدی صرف کامل کردن طراحی وولتا و حل این مشکلات شد.
تعمیرات پیل وولتا
ویلیام کریکشنک از اسکاتلند با قرار دادن پیل وولتا در کنار آن به شکل”خنک کننده باتری” مشکل نشت را حل کرد.
مشکل دوم”طول عمر کوتاه” ناشی از تخریب روی بعلت ناخالصی ها و ایجاد حباب های هیدروژنی بر روی مس بود.
ویلیام استورژون در سال ۱۸۳۵ کشف کرد که افزودن زینک به جیوه از تخریب جلوگیری می کند.
شیمیدان بریتانیایی “جان فردریک دنیل ” از یک الکترولیت دیگر که با هیدروژن واکنش می داد، برای جلوگیری از انباشته شدن روی کاتد مس استفاده کرد.
باتری دو الکترولیتی دنیل، که بعنوان سلول دنیل شناخته می شود،تبدیل به یک راه حل بسیار محبوب برای ارایه قدرت به شبکه های تلگراف تازه تاسیس شد.
اولین باتری قابل شارژ
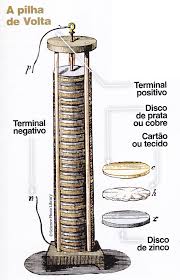
در سال ۱۸۵۹ ، فیزیکدان فرانسوی گاستون پلنت ، یک باتری را با استفاده از دو ورق نورد سرب که در اسید سولفوریک غوطه ور بود،ساخت.
با تغییر جریان الکتریسیته از طریق باتری ، شیمی به حالت اولیه خود باز می گردد،بنابراین اولین باتری قابل شارژ را ایجاد می کند.
بعدها، در سال ۱۸۸۱، کامیل الفونس فور ، طراحی صفحات را با تشکیل ورق های سرب به صفحات بهبود داد.
این طراحی باتری را ساده تر ساخت و از باتری اسید سرب در خودروها استفاده گسترده ای شد.
باتری خشک
تا اواخر دهه ۱۸۰۰ ، الکترولیت در باتری ها ، در حالت مایع بود.
این امر، حمل بار الکتریکی را بسیار محتاطانه می کرد و اکثر باتری ها هرگز برای حرکت و اتصال به مدار در نظر گرفته نشدند.
در سال ۱۸۶۶ ، ژرژ لکنان یک باتری را با استفاده از یک آند روی ، یک کاتدی دی اکسید منگنز و یک محلول آمونیوم کلرید برای الکترولیت ایجاد کرد.
درحالی که الکترولیت هنوز در سلول leclanche مایع بود، شیمی باتری ثابت کرد که یک گام مهم برای اختراع باتری خشک است.
کارل گاسنر چگونگی ایجاد یک الکترولیت خارج از کلرید آمونیوم و گچ پاریس را کشف کرد.
او در سال ۱۸۸۶ در آلمان باتری خشک جدید را اختراع نمود.
این باتریهای خشک جدید که معمولا “باتری های روی کربن” نامیده می شوند، فراوان تولید شدند و تا اواخر دهه ۵۰ میلادی بسیار به محبوبیت رسیدند.
در حالی که کربن در واکنش شیمیایی استفاده نمی شود، نقش مهمی را به عنوان یک هادی الکتریکی در باتری روی-کربن بازی می کند.
در دهه ۱۹۵۰، لوئیس اری، پل مارشال و کارل کوردش از شرکت اتحادیه کاربید (که بعدها به عنوان “Eveready” و سپس “Energizer” شناخته شد) الکترولیت کلرید آمونیوم را با یک ماده قلیایی ، بر اساس شیمی باتری فرموله شده توسط والدیمر جانگنر در سال ۱۸۹۹، جایگزین کردند. باتری های خورشیدی قلیایی می توانند انرژی بیشتری از باتری های کربنی روی، در همان اندازه، نگهدارند و عمر مفیدتری داشته باشند.
باتری های قابل شارژ قرن بیست و یکم
در دهه ۱۹۷۰ COMSAT باتری نیکل هیدروژن را برای استفاده در ماهواره های ارتباطی توسعه داد.
این باتری ها هیدروژن را در قالب گازدار تحت فشار ذخیره می کنند.
بسیاری از ماهواره های ساخته ی دست انسان، مانند ایستگاه فضایی بین المللی هنوز روی باتری های نیکل هیدروژن تکیه می کنند.
تحقیق از چندین شرکت از اواخر دهه ۱۹۶۰ منجر به تولید باتری نیکل هیدرید متال (NiMH) شد.
باتری های NiMH در سال ۱۹۸۹ به بازار مصرف کننده عرضه شدند و جایگزینی کوچکتر و ارزان تر را برای باتری های هیدروژن نیکل قابل شارژ فراهم کردند.
شیمی Asahi از ژاپن نخستین باتری لیتیوم یون را در سال ۱۹۸۵ و سونی اولین باتری لیتیوم یون را در سال ۱۹۹۱ ساخت. در اواخر دهه ۱۹۹۰ یک پوشش نرم و انعطاف پذیر برای باتری های لیتیوم یون ساخته و باعث ایجاد ” باتری لیتیوم پلیمر “یا ” LiPo ” شد.








2 دیدگاه
ممنون از پست خوبتون
موضوع سئوال : باتری چیست ؟
خواهش می کنم باعث افتخار ما شدید
موضوع سئوال : باتری چیست؟