- تماس با ما
- 09121001976
- parspalma@gmail.com

سلول سوختی آلکالاین
۱۳۹۸-۰۱-۲۶
سلول سیلندری
۱۳۹۸-۰۱-۲۶باتری گردشی
باتری گردشی یا باتری گردشی ردوکس (پس از کاهش اکسیداسیون) یک نوع سلول الکتروشیمیایی است که در آن انرژی شیمیایی توسط دو جزء شیمیایی که در مایعات موجود در سیستم حل و از طریق یک غشا جدا شده، مجهز شده است. تبادل یونی (همراه با گردش جریان الکتریکی) از طریق غشاء رخ می دهد در حالی که هر دو مایعات در فضای مربوطه خود به گردش درمی آیند.
یک باتری جریان می تواند مانند یک سلول سوختی (که در آن سوخت مصرف شده استخراج می شود و سوخت جدید به سیستم اضافه می شود) یا مانند یک باتری قابل شارژ (که در آن یک منبع برق، باعث احیای سوخت می شود) استفاده می شود.
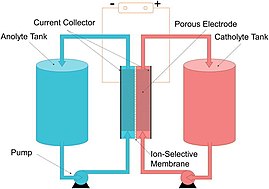
باتری گردشی ۱
اصل ساختار
باتری گردشی یک سلول سوختی قابل شارژ است که در آن یک الکترولیت حاوی یک یا چند عنصر الکتریکی حل شده که از یک سلول الکتروشیمیایی که به طور برگشتی انرژی شیمیایی را به طور مستقیم به برق تبدیل می کند، جریان می یابد (عناصر الکتریکی عبارتند از: عناصر موجود در محلول که می توانند در واکنش الکترود شرکت کنند یا می توانند بر روی الکترود جذب شوند). الکترولیت اضافی به صورت خارجی ذخیره می شود، عموما در تانک ها، و معمولا از طریق سلول (یا سلول های) راکتور پمپ می شود
انواع
انواع مختلفی از باتری های گردشی توسعه یافته اند، از جمله ردوکس، هیبرید و غشایی. تفاوت اساسی بین باتری های معمولی و باتری گردشی ، این است که انرژی به عنوان مواد الکترود در باتری های معمولی ذخیره نمی شود، بلکه به عنوان الکترولیت در باتری گردشی است.
ردوکس
سلول ردوکس (اکسیداسیون کاهشی) یک سلول برگشت پذیر است که در آن اجزای الکتروشیمیایی در الکترولیت حل می شوند. باتری های گردشی ردوکس قابل شارژ (سلول های ثانویه) هستند.
نمونه هایی از باتری های گردشی ردوکس عبارتند: از باتری گردشی ردوکس وانادیوم، باتری برومید پلی سولفید (Regenesys) و باتری گردشی ردوکس اورانیوم. سلول های سوختی ردوکس کمتر تجاری هستند.
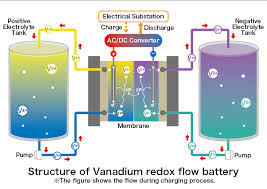
باتری گردشی ۲
هیبرید
باتری گردشی هیبریدی از یک یا چند جزء الکتریکی استفاده می کند که به عنوان یک لایه جامد به حساب می آیند. در این مورد، سلول الکتروشیمیایی شامل یک الکترود باتری و یک الکترود سلول سوختی است. باتری های گردشی هیبریدی شامل زینک بروم، روی سریم، سرب اسید و باتری های گردشی iron-salt هستند.
غشایی
یک باتری غشایی به جریان لمینری متصل می شود که در آن دو مایع از طریق یک کانال پمپ می شوند، جایی که واکنش های الکتروشیمیایی برای ذخیره یا آزاد شدن انرژی انجام می شوند. جریان به طور طبیعی مایعات را جدا می کند و نیاز به غشا را از بین می برد.
غشاء ها اغلب گران ترین جزء باتری هستند و کمتر از باقی اجزاء قابل اعتماد اند. عدم وجود یک غشاء امکان استفاده از محلول بروم مایع و هیدروژن را فراهم میکند: این ترکیب هنگام استفاده از غشاء مشکل ساز می شود، زیرا آن ها اسید هیدروبرومیک را تشکیل می دهند که می توانند غشاء را از بین ببرند. هردو مواد با هزینه کم در دسترس هستند.
آلی
در مقایسه با باتری های گردشی ردوکس سنتی آبی غیر آلی، مانند باتری های گردشی ردوکس وانادیم و باتری های Zn-Br2، که پس از چندین دهه توسعه یافته اند، باتری های گردشی آلی ردوکس در سال ۲۰۰۹ ظهور کردند.
متال هیدرید
باتری گردشی پروتون (PFB) الکترودهای ذخیره سازی متال هیدرید را به یک سلول سوختی غشایی تبادل پروتون (PEM) متصل می کند. در طول شارژ، PFB، یون های هیدروژن تولید شده از آب شکافته شده با الکترون ها و ذرات فلزی را در یک الکترود از یک سلول سوختی ترکیب می کند. انرژی در قالب متال هیدرید در حالت جامد ذخیره می شود. دشارژ هنگامی که روند معکوس می شود و پروتون ها با اکسیژن محیط ترکیب می شوند، برق و آب تولید می کند. فلزات ارزان تر از لیتیوم می توانند مورد استفاده قرار گیرند و تراکم انرژی بیشتری نسبت به سلول های لیتیوم تولید کنند.
شبکه نانو
سیستم لیتیوم سولفور قرار داده شده در یک شبکه از ذرات نانو نیاز به جابجایی شارژ در داخل و خارج از ذرات که در تماس مستقیم با یک صفحه هدایت شده اند را از بین می برد. در عوض، شبکه ذرات نانو اجازه می دهد که برق در سراسر مایع جریان یابد. این اجازه می دهد تا انرژی بیشتری استخراج شود.
نیمه جامد
در یک باتری گردشی نیمه جامد، الکترود های مثبت و منفی از ذرات معلق در یک مایع حامل تشکیل شده اند. تعلیقات مثبت و منفی در تانک های جداگانه ذخیره می شوند و از طریق لوله های جداگانه به دسته ای از اتاق های مجاور واکنش پمپ می شوند، که از طریق یک مانع مانند غشای نازک و متخلخل جدا می شوند.
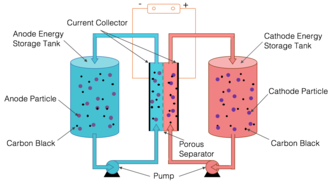
باتری گردشی ۳
مزایا
باتری های گردشی ردوکس و باتری های گردشی هیبریدی کم وسعت تر، دارای مزایای طرح های انعطاف پذیر هستند ( به علت جدایی اجزای قدرت و انرژی)، چرخه عمر طولانی (به دلیل عدم انتقال فاز جامد به جامد)، سریع بودن زمان های پاسخگویی، بدون نیاز به شارژ “برابری” ( شارژ بیش از حد باتری برای اطمینان ازینکه همه سلول ها شارژ برابر دارند) و هیچ انتشار مضری ندارند.