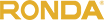- تماس با ما
- 09121001976
- parspalma@gmail.com

انرژی جنبشی
۱۳۹۸-۰۴-۱۰
انرژی پتانسیل
۱۳۹۸-۰۴-۱۰انرژی آزاد گیبس
در ترمودینامیک، انرژی آزاد گیبس یک پتانسیل ترمودینامیکی است که می تواند برای محاسبه حداکثر کار برگشت پذیر که ممکن است انجام شود، به کار گرفته شود. این حداکثر کار برگشت پذیر توسط سیستم های ترمودینامیکی با دمای ثابت (ایزوترمال) و فشار ثابت انجام پذیر است. (نام های توصیه شده برای انرژی آزاد گیبس توسط IUPAC، انرژی گیبس یا تابع گیبس هستند. همچنین به عنوان آنتالپی آزاد نیز شناخته می شود تا به این سبب بتوان آن را از انرژی آزاد هلمولتز تشخیص داد.)
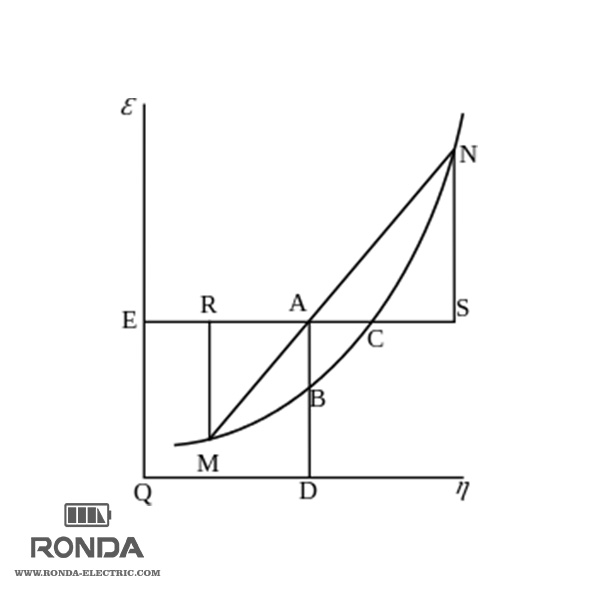
انرژی آزاد گیبس به صورت ΔG = ΔH – TΔS محاسبه می شود و در واحد استاندارد اندازهگیری، یکای آن ژول است.
انرژی آزاد گیبس، حداکثر مقدار کار غیر انبساطی است که می تواند از یک سیستم ترمودینامیکی بسته بدست آید. سیستم ترمودینامیکی بسته سیستمی است که می تواند تبادل گرما و کار با محیط اطراف خود داشته باشد اما تبادل ماده در آن رخ نمی دهد. حداکثر کار غیر انبساطی نیز می تواند تنها در یک فرایند کاملا برگشت پذیر به دست آید. هنگامی که یک سیستم برگشت پذیر از یک حالت اولیه به حالت نهایی تبدیل می شود، کاهش انرژی آزاد گیبس برابر کارهایی است که سیستم روی محیط اطراف خود اعمال می کند. این مقدار برابر است با منفی کاری که نیروهای فشار از محیط به سیستم وارد می کنند.
انرژی گیبس (که با نماد G نمایش داده می شود) نیز پتانسیل ترمودینامیکی است. این پتانسیل ترمودینامیکی زمانی به حداقل مقدار خود می رسد که سیستم در فشار و دمای ثابت به تعادل شیمیایی رسیده باشد. تغییرات این پتانسیل در نقطه تعادل صفر می شود. به همین ترتیب، کاهش G یک شرط لازم برای ایجاد فرایندهای خود بخودی در فشار و دمای ثابت است.
انرژی آزاد گیبس در دهه ی ۱۸۷۰ برای اولین بار توسط دانشمند آمریکایی، جوزیا ویلارد گیبس (Josiah Willard Gibbs)، با نام “انرژی در دسترس” معرفی شد. در سال ۱۸۷۳، گیبس این انرژی را به صورت زیر توصیف کرد:
” بزرگترین مقدار کار مکانیکی است که می توان از مقدار معینی از یک مادهی خاص با شرایط اولیه داده شده، به دست آورد. این مقدار بدون افزایش حجم کل آن و بدون انتقال گرما به داخل سیستم و یا ورود انرژی از خارج سیستم به دست می آید.”
بررسی اجمالی
طبق قانون دوم ترمودینامیک، برای سیستم های واکنشی در STP (یا هر سیستم با دمای ثابت و فشار ثابت دیگری)، یک گرایش عمومی طبیعی برای دستیابی به حداقل انرژی آزاد گیبس وجود دارد.
در اندازه گیری های کمی، مطلوب از یک واکنش داده شده در دمای ثابت و فشار ثابت، به دست آوردن تغییرات انرژی آزاد گیبس است که در آن واکنش آزاد شده است. این کمیت با ΔG نمایش داده می شود، که البته گاهی اوقات نیز به صورت “دلتا G” یا “dG” نوشته می شود. به عنوان یک شرط لازم برای واکنش در دما و فشار ثابت، ΔG باید از کارهای غیر فشاری (کاری که از اعمال فشار بر روی سیستم به دست نیاید به عنوان مثال کار الکتریکی) اعمال شده بر روی سیستم کوچکتر باشد که اغلب این مقدار در کار های غیر فشاری برابر صفر است از این رو ΔG باید منفی باشد. ΔG برابر با حداکثر مقدار کار غیر فشاری است که می تواند به عنوان یک نتیجه از واکنش شیمیایی در مورد یک فرآیند برگشت پذیر انجام شود.
تاریخچه
کمیتی به نام “انرژی آزاد” جایگزین پیشرفته تر و دقیق تری است نسبت به مفهومی که قبل از ایجاد شیمی فیزیکی برای توصیف نیرویی که باعث واکنش های شیمیایی شده بود، استفاده می شد.
ویلارد گیبس در سال ۱۸۷۳ روش شناخت هندسی خواص ترمودینامیکی مواد با استفاده از سطوح را منتشر کرد که در آن اصول معادله جدید خود را طرح کرد. این اصول جدید قادر بود تا به پیش بینی یا برآورد گرایش های مختلف فرآیندهای طبیعی در حالتی که سیستم ها در تماس با یکدیگر هستند، بپردازد. با بررسی تعاملات مواد همگن در تماس با یکدیگر، یعنی اجسام متشکل از بخشی جامد، بخشی مایع و بخشی بخار، و با استفاده از یک نمودار انرژی سه بعدی آنتروپی، گیبس توانست سه حالت تعادل را به دست آورد. این سه حالت شامل حالت های “لزوما پایدار”، “خنثی” و “ناپایدار” بودند که می توانست توضیح دهد آیا در هر یک از این حالت ها تغییرات ایجاد می شود یا در گذر زمان هم ثابت می مانند.
پس از آن، در سال ۱۸۸۲، هرمان فون هلمولتز (Hermann von Helmholtz)، دانشمند آلمانی، بزرگترین مقدار کار که ممکن است وقتی که واکنش به روش برگشت پذیر انجام می شود به دست آید، مانند کار الکتریکی در یک سلول (باتری) برگشت پذیر را نشان داد.
بنابراین حداکثر کار به عنوان کاهش انرژی آزاد یا انرژی موجود در سیستم در نظر گرفته می شود. (انرژی آزاد گیبس در دمای ثابت، فشار ثابت و یا به تعریفی دیگر انرژی آزاد هلمهولتز با نماد F در دما و حجم ثابت) بنابراین، G یا F مقدار انرژی “آزاد” برای کار تحت شرایط داده شده است.