- تماس با ما
- 09121001976
- parspalma@gmail.com

سلول Leclanche
۱۳۹۸-۰۲-۲۱
جریان الکتریکی
۱۳۹۸-۰۲-۲۱آند
آند یک الکترود است که از طریق آن جریان قراردادی وارد یک دستگاه الکتریکی میشود.
آند قطب مخالف کاتد است، کاتد یک الکترود است که از طریق آن، جریان قراردادی دستگاه الکتریکی را ترک میکند.
جهت جریان قراردادی (جریان بارهای مثبت) در یک مدار مخالف جهت جریان الکتریکی است، بنابراین الکترونها (بار منفی) از آند به کاتد جریان مییابند.
در یک سلول گالوانیکی، آند الکترودی است که در آن واکنش اکسیداسیون اتفاق میافتد.
جریان شارژ
اصطلاح آند و کاتد توسط ولتاژ الکترود تعریف نمیشود، بلکه جهت جریان از طریق الکترود است که این دو را تعریف میکند.
آند، الکترودی است که از طریق آن جریان قراردادی (بار مثبت) از مدار خارجی به داخل دستگاه جریان مییابد، در حالی که کاتد الکترودی است که جریان قراردادی از آن خارج میشود.
اگر جریان از طریق الکترودها جهت را عوض کند، به عنوان مثال یک باتری قابل شارژ زمانی که شارژ میشود، نام گذاری الکترودها به عنوان آند و کاتد برعکس میشود.
تعریف آند و کاتد برای دستگاه های الکتریکی مانند دیودها و لوله های خلاء که در آن نامگذاری الکترود ثابت است، کمی متفاوت است و به جریان واقعی (قراردادی) بستگی ندارد.
آندهای الکترولیتی
در الکتروشیمی، آند جایی است که اکسیداسیون رخ میدهد و با قطبی مثبت در یک سلول الکترولیتی در تماس است.
در آند آنیونها (یون های منفی) به وسیله پتانسیل الکتریکی وادار میشوند تا به صورت شیمیایی واکنش دهند و الکترونها را از دست بدهند (اکسیداسیون) تا در مدار جریان یابند.
این فرایند به طور گسترده ای در پالایش فلزات مورد استفاده قرار میگیرد.
به عنوان مثال در تصفیه مس، آندهای مس در یک محلول مناسب (مانند اسید سولفوریک) الکترولیز میشوند تا کاتدهای با خلوص بالا (۹۹/۹۹ درصد) را تولید کنند.
کاتدهای مس تولید شده با استفاده از این روش نیز به عنوان الکترولیتیک مس نامیده میشوند.
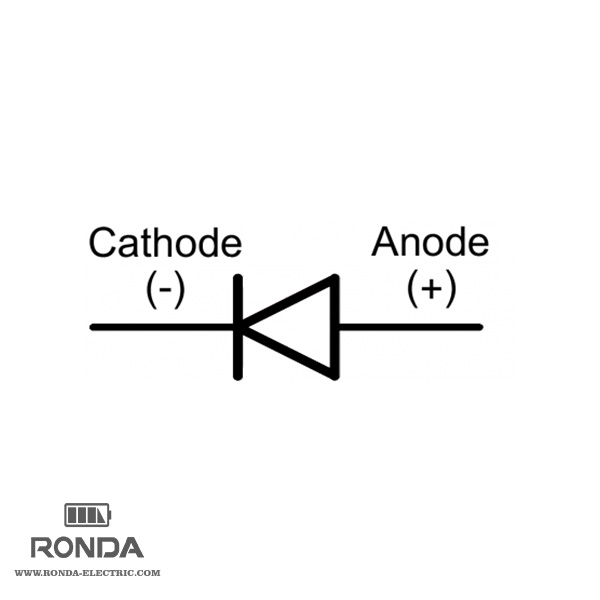
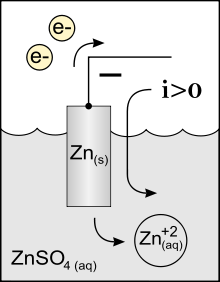
آند باتری ها و سلولهای گالوانیک
در یک باتری یا سلول گالوانیزه، آند الکترودی منفی است که از آن الکترون به طرف خارجی قسمت مدار جریان می یابد.
در داخل سیستم کاتیون های بار دار تمایل دارند تا از آند فاصله بگیرند ( اگرچه بار این دو مخالف یکدیگر است از این رو انتظار میرود که یکدیگر را جذب کنند، ولی این رفتار، به علت پتانسیل الکترودها نسبت به محلول الکترولیت است که برای آند و کاتدهای الکترولیتی و فلزی متفاوت است).
بر خلاف این پدیده خارج از سلول در مدار، الکترون ها تحت فشار قرار میگیرند و بنابراین به وسیلهی ولتاژ اعمال شده در مدار جریان پیدا میکنند.در ایالات متحده، بسیاری از تولیدکنندگان باتری، الکترود مثبت را ، به ویژه در ادبیات فنی خود، به عنوان آند می دانند.
اگر چه از لحاظ فنی نادرست است، مشکل اینکه کدام یک از الکترودها آند باشد را در یک سلول ثانویه (یا قابل شارژ) حل میکنند.
آند در لوله خلاء
در دستگاه های الکترونیکی خلاء مانند یک لوله پرتو کاتدی، آند که با بار مثبت شارژ شده است، الکترونها را جذب خود میکند. در این لوله، آند یک صفحه با بار مثبت است که الکترون هایی را که از کاتد منتشر شده اند از طریق جذب الکتریکی جمع میکند و همچنین جریان این الکترونها را تسریع می بخشد.
آندهای محافظ
در حفاظت کاتدی، یک آند فلزی که بیشتر به محیط تخریب گر (دربارهی فلزاتی که زنگ می زنند) اطراف خود واکنش نشان میدهد برای محافظت، به سیستم مورد نظر متصل میشود و ممکن است بخشی از زنگ زده و یا حل شود تا از فلز اصلی سیستم متصل به آن محافظت کند.
به عنوان مثال، یک بدنه کشتی آهنی یا فولادی ممکن است از طریق یک آند محافظ از جنس روی محافظت شود، به این صورت که این آند در داخل آب دریا حل میشود و از زنگ زدگی بدنه کشتی جلوگیری میکند.
آندهای محافظ به مخصوص برای سیستم هایی مورد نیاز است که در آن یک بار استاتیک به وسیله ی عبور مایعات جاری ایجاد میشود که به عنوان مثال میتوان خطوط لوله و بدنه ی کشتیها را نام برد.
این نوع از آندها به طور معمول در مخزن آب گرمکن ها نیز مورد استفاده قرار میگیرند.
در سال ۱۸۲۴، دانشمند مهندس هومفری دیوی، برای کاهش تاثیر این مخرب های زیر آب بر روی کشتی ها، تمامی تجهیزات زیر آب را به وسیله ی این آندها پوشش داد.
روشی که وی توسعه داد اولین سیستم حفاظت الکترولیز دریایی در حال حاضر است که امروزه نیز به طور گسترده مورد استفاده قرار میگیرد.
دیوی آندهای محافظ را از جنس یک فلز که واکنش پذیری بالای الکتریکی داشت ساخت و آن را به بدنه کشتی متصل کرد و با اتصال الکتریکی به یک مدار متصل کرد تا محفاظت کاتدی را بر روی تجهیزات کشتی اعمال کند.
یک نمونه دیگر از موارد کاربردی از این نوع حفاظت که کمتر به آن توجه میشود، فرآیند گالوانیزه کردن آهن است.
این فرآیند سازه های آهنی (مانند شمشیرهای مورد استفاده در شمشیربازی) را با پوشش فلز روی محافظت میکند و در این صورت تا زمانی که روی باقی بماند، آهن از اثرات خوردگی محافظت میشود.