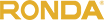- تماس با ما
- 09121001976
- parspalma@gmail.com

باتری خودرو های الکتریکی
۱۳۹۸-۰۲-۱۸
آند
۱۳۹۸-۰۲-۱۸سلول Leclanche
سلول Leclanche یک باتری اختراع و ثبت شده توسط دانشمند فرانسوی جرج لکلانچه در سال ۱۸۶۶ است.
این باتری حاوی محلول رسانای (الکترولیت) آمونیوم کلرید, یک کاتد (پایانه مثبت) کربن, اکسید کننده دی اکسید منگنز (اکسیدکننده) و آند (ترمینال منفی) روی (کاهش دهنده) بود. شیمی این سلول در آینده برای تولید یک سلول خشک با موفقیت سازگار شد.
تاریخچه
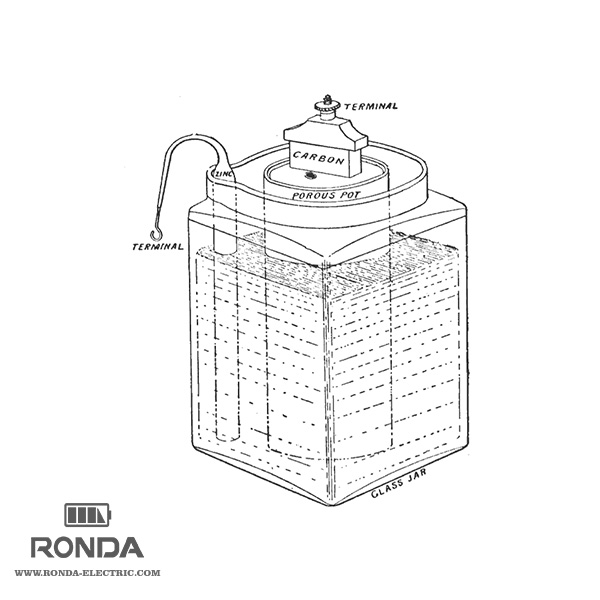
در سال ۱۸۶۶، جرج Leclanche یک باتری را اختراع کرد که شامل آند روی و کاتد دی اکسید منگنز پیچیده شده دریک ماده متخلخل ، در شیشه ای از محلول آمونیوم کلرید غوطه ور بود.
کاتد دیاکسید منگنز یک کربن کوچک مخلوط شده داشت که رسانایی و جذب را بهبود می بخشید. این، ولتاژ ۱.۴ ولت را تامین می کرد.
این سلول در تلگراف، سیگنال دهی و عملکرد زنگ برقی به موفقیت بسیار سریعی دست یافت.
شکل سلول خشک برای نیرو بخشیدن به تلفن های اولیه ( معمولا از جعبه ای چوبی و مجاور به دیوار استفاده می شده است) قبل از آنکه تلفن بتواند قدرت خود را از طریق خط تلفن به دست آورد. سلول Leclanche نمی تواند جریان مداوم را برای زمانی طولانی فراهم کند.
در مکالمه های طولانی، عملکرد باتری کاهش می باید و مکالمه نارسا و نامفهوم می شود.
ساختار
شکل اصلی این سلول از یک محفظه متخلخل استفاده کرده است. این به آن، مقاومت داخلی نسبتاً بالایی بخشید و اصلاحات متعددی برای کاهش آن انجام شد.این ها شامل “سلول بلوکی آگلومرا” و “سلول کیسه ای” بودند.
در ابتدا لکلانچه ، و پس از او کارل گسنر هر دو در تلاش بودند تا سلول مرطوب اصلی را به یک سلول خشک قابل حمل تر و کارآمد تر تبدیل کنند.
سلول متخلخل محفظه ای
در سلول اصلی Leclanche عامل اکسید کننده در سلول که شامل دی اکسید منگنز خرد شده است ، در یک محفظه بسته بندی شد و یک میله کربن به عنوان کاتد(واکنش کاهشی) وارد عمل شد. پس از آن آند(واکنش اکسیداسیون) که یک میله روی بود، به همراه محفظه در محلول آمونیوم کلرید غوطه ورشد.
محلول مایع به عنوان الکترولیت عمل کرد و در داخل محفظه متخلخل نفوذ کرد تا با کاتد تماس پیدا کند.
سلول بلوکی متراکم شده
در سال ۱۸۷۱ Leclanche استفاده از محفظه متخلخل را متوقف کرد و یک جفت بلوک متراکم شده را جایگزین آن کرد که توسط نوارهای لاستیکی به صفحه کربن متصل می شد.
صفحه کربن با باندهای لاستیکی تعویض کرد. این بلوکها با مخلوط کردن دی اکسید منگنز با عوامل لازم و فشار دادن مخلوط به قالب ساخته شدند.
سلول های کیسه ای
در این سلول، محفظه متخلخل با بسته بندی ای از پارچه برزنت یا گونی جایگزین شد. علاوه بر این، میله روی با یک سیلندر روی جایگزین شد تا به یک سطح بزرگ تر برسد. این، مقاومت داخلی پایین تری را نسبت به مواد فوق(متخلخل و متراکم) داشت.
اضافه کردن نشاسته
در سال ۱۸۷۶ جرج Leclanche با تقلا نشاسته را به الکترولیت کلرید آمونیوم اضافه کرد تا حالت ژله ای بهتری داشته باشد.
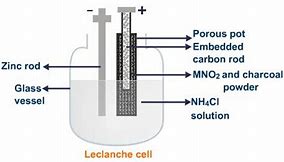
سلول خشک بهبود یافته
در سال ۱۸۸۸، یک پزشک آلمانی، کارل گسنر فرایند ژله ای شدن را بهبود بخشید و سلول خشک قابل حمل تری را با مخلوط کردن گچ و مواد شیمیایی اب دوست با الکترولیت کلرید آمونیوم تولید کرد.
شیمی
واکنش ردوکس در سلول Leclanche شامل دو نیمه واکنش زیر است:
_آند (اکسیداسیون روی): Zn → Zn2+ + 2e
_کاتد(کاهش Mn(iv) )
۲ MnO2 + 2NH4+ + 2e− → ۲ MnO(OH) + 2 NH3
فرایند شیمیایی که برق را در یک سلول Leclanche تولید می کند، زمانی شروع می شود که اتم های روی، روی سطح آند آن را اکسید کنند، یعنی هر دو الکترون خود را از دست بدهند تا یون های Zn2+ مثبت بمانند.
هنگامی که سلول در یک مدار الکتریکی خارجی متصل می شود، الکترون های اضافی برروی آند روی از طریق مدار به سمت میله کربن جریان می یابند، این حرکت الکترون ها جریان الکتریکی را شکل می دهد.
پس از گذر از کل مدار، هنگامی که الکترون ها به کاتد( میله کربن) وارد می شوند، با دی اکسید منگنز (MnO2) و آب (H2O) ترکیب می شوند که برای تولید اکسید منگنز (Mn2O3) و یون های هیدروکسید منفی با یکدیگر واکنش می دهند.
کاربرد ها
نیروی الکتروموتیو (e.m.f) تولید شده توسط یک سلول ۱٫۴Leclanche ولت است، با مقاومتی چندین اهمی که در آن یک محفظه متخلخل استفاده می شود.
استفاده گسترده ای از آن در تلگراف، سیگنال دهی، زنگ های الکتریکی و کاربرد های مشابه دیگر که در آن جریان متناوب مورد نیاز بود و مطلوب بود که باتری باید به کمی نگهداری و تعمیر نیاز داشته باشد.
سلول مرطوب باتری لکلانچه پیشرو یک باتری مدرن روی کربن (سلول خشک) بود. اضافه کردن روی کلرید به خمیر الکترولیت e.m.f. را تا ۱.۵ ولت بالا برد.
پیشرفت های بعدی استفاده ازآمونیوم کلرید را به طور کامل باطل کرد، و سلولی ارائه کرد که می توانست بدون مقاومت داخلی خود که به سرعت بالا می رفت، دشارژ پایدار تری را تحمل کند.(سلول روی کلرید)