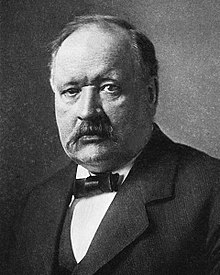- تماس با ما
- 09121001976
- parspalma@gmail.com

Fluidic Energy
۱۳۹۸-۰۲-۳۰
انرژی های تجدید پذیر
۱۳۹۸-۰۲-۳۰الکترولیت
الکترولیت مادهای است که هرگاه در حلال قطبی مانند آب حل شود، رسانای الکتریکی تولید میکند.
الکترولیت حل شده به کاتیون ها و آنیون هایی جدا می شود که از طریق حلال پخش میشوند. از نظر الکتریکی چنین محلولی خنثی است.
اگر یک پتانسیل الکتریکی بر چنین محلولی اعمال شود کاتیون های محلول به سمت الکترودی که دارای فراوانی الکترون است، جاری می شوند و این در حالی است که آنیون ها به سمت الکترودی جذب می شوند که کسری الکترون داشته باشد.
حرکت آنیون ها و کاتیون ها در جهت مخالف در این محلول به یک جریان الکتریکی می انجامد. بیشتر این محلول ها شامل نمک های حل شونده و اسید ها می باشند. همچنین بعضی از گازها مانند کلرید هیدروژن، در شرایط دمای بالا یا فشار کم می توانند به عنوان الکترولیت عمل کنند.
محلولهای الکترولیتی همچنین میتوانند از انحلال برخی از پلیمر های بیولوژیکی ( مثل DNA ) و پلیمرهای مصنوعی ( مثل پلی استایرن سولفونات) حاصل شوند. مادهای که به محلول یونی تبدیل میشود، ظرفیت تولید برق را به دست میآورد.
سدیم، پتاسیم، کلرید، کلسیم، منیزیم و فسفات نمونه هایی از الکترولیت ها هستند. ریشه لغت کلمه الکترولیت از واژه ی یونانی به معنی ” قادر به جدا شدن یا خنثی کردن” به دست می آید.
تاریخچه
آوانت آرننیوس (Svante Arrhenius) در رساله ی خود که در سال ۱۸۸۴ نوشت، توضیح داد که نمک های کریستال جامد هنگام انحلال به شکل جفت ذرات باردار از هم جدا میشوند که به همین سبب وی جایزه نوبل شیمی سال ۱۹۰۳ را کسب کرد.
وی اینگونه توضیح داد که در تشکیل یک محلول، نمک به ذرات باردار تبدیل میشود که مایکل فارادی چند سال پیش این ذرات باردار را “یون” نامید.
فارادی اعتقاد داشت که این یون ها در فرآیند الکترولیزاسیون تولید میشوند. آرتنیوس ادعا کرد که حتی در صورت عدم جریان الکتریکی، محلول های نمک حاوی یون هستند.
شکل گیری
محلول الکترولیتی معمولا هنگامی تشکیل می شود که یک نمک به یک حلال تبدیل شود مانند زمانی که مولکول ها در آب در فرآیندی به نام انحلال به علت تعامل ترمودینامیکی بین حلال و مولکول های محلول جدا میشوند.
به عنوان مثال، هنگامی که نمک طعام (کلرید سدیم NaCl ) در آب قرار میگیرد، با توجه به واکنش تجزیه ،نمک (جامد) به یون های خود تجزیه می شود.
همچنین ممکن است برای تولید یون ها واکنش با آب صورت گیرد. به عنوان مثال، گاز دی اکسید کربن در آب حل می شود تا محلولی حاوی هیدرونیوم، کربنات و یون های کربنات هیدروژن تولید کند.
نمک های مذاب نیز میتوانند الکترولیت باشند، به عنوان مثال وقتی که کلرید سدیم مذاب می شود، مایعی رسانا تولید میکند.
به طور خاص، مایعات یونی که نمک های مذاب با نقطه ذوب کمتر از ۱۰۰ درجه سانتیگراد هستند، نوعی از الکترولیت های غیر آبی بسیار رسانا هستند و در نتیجه کاربرد بیشتری در سلول های سوختی و باتری ها پیدا کرده اند.
اهمیت فیزیولوژیکی
در فیزیولوژی، یون های اولیه الکترولیت ها عبارتند از سدیم (Na +)، پتاسیم (K +)، کلسیم (Ca2 +)، منیزیم (Mg2 +)، کلرید (Cl-)، هیدروژن فسفات (HPO42-) و کربنات هیدروژن (HCO3-).
نماد بار الکتریکی مثبت (+) و منفی (-) نشان میدهد که ماده، یونی و دارای توزیع نامتقارن الکترون ها است، نتیجه ی انحلال شیمیایی می باشد.
سدیم، الکترولیت اصلی در مایع خارج سلولی است و پتاسیم، الکترولیت درونی سلولی میباشد که هر دو در تعادل مایع و کنترل فشار خون دخالت دارند.
تمام فرم های زندگی شناخته شده، نیاز به تعادل الکترولیتی ظریف و پیچیده بین محیط های داخل سلولی و خارج سلولی دارند. مکانیزم های مختلف موجودی در گونه های زنده وجود دارد که غلظت الکترولیت های مختلف را تحت کنترل شدید نگه می دارند.
بافت های عضلانی و نورون ها، مانند بافت های الکتریکی بدن در نظر گرفته میشوند. عضلات و نورون ها با فعالیت الکترولیت های موجود در مایع خارج سلولی، مایع بینابینی و مایع داخل سلولی فعال می شوند.
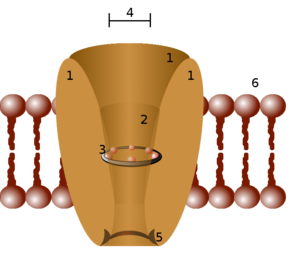
الکترولیت ها میتوانند از طریق ساختار های پروتئینی تخصصی که در غشای پلاسما به نام “کانالهای یونی” تعبیه شده اند، به سلول وارد شده یا از غشای سلولی خارج شوند.
به عنوان مثال، انقباض عضله بستگی به حضور کلسیم (Ca2 +)، سدیم (Na +) و پتاسیم (K +) دارد. بدون سطح کافی این الکترولیت های کلیدی، ممکن است ضعف عضلانی یا انقباض شدید عضلات رخ دهد.
الکتروشیمی وقتی الکترود ها در یک الکترولیت قرار میگیرند و به آن ها ولتاژ اعمال می شود، الکترولیت الکتریسیته را هدایت میکند. الکترون ها به تنهایی نمیتوانند از درون الکترولیت عبور کنند. در عوض واکنش شیمیایی در کاتد اتفاق میافتد و الکترون ها به الکترولیت منتقل میشوند و واکنش بعدی در آند رخ میدهد که الکترونها را از الکترولیت جذب میکند.
در نتیجه، ابری از بارهای منفی در الکترولیت اطراف کاتد ایجاد می شود و ابری از بار مثبت نیز در اطراف آند جمع میشود. یون ها در الکترولیت این بار ها را خنثی میکنند و الکترون ها را به جریان می اندازند و باعث می شوند تا واکنش ها ادامه یابند.