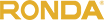- تماس با ما
- 09121001976
- parspalma@gmail.com

انرژی آزاد هلمهولتز
۱۳۹۸-۰۴-۲۲
هم ارزی جرم و انرژی
۱۳۹۸-۰۴-۲۲انرژی درونی
در ترمودینامیک انرژی داخلی یک سیستم، کل انرژی موجود در سیستم است. این انرژی برای ایجاد یا آماده سازی سیستم در هر حالت خاص لازم است. اما این انرژی درونی نه شامل انرژی جنبشی سیستم است که از حرکت کل سیستم ناشی می شود. و نه شامل انرژی پتانسیل سیستم است که به دلیل اعمال نیروهای خارجی از محیط اطراف سیستم به آن وارد می شوند.
انرژی درونی تنها شامل انرژی هایی است که به دلیل تغییر وضعیت داخلی سیستم ممکن است از دست برود و یا به دست بیاید.
انرژی داخلی یک سیستم را می توان با معرفی ماده، به وسیله ی اعمال حرارت و یا انجام کار ترمودینامیکی بر روی سیستم، افزایش داد.
هنگامی که دیواره های نفوذ ناپذیر مانع از انتقال ماده می شوند، گفته می شود که سیستم بسته است. و نخستین قانون ترمودینامیک می تواند به عنوان تعریف انرژی داخلی به عنوان مجموع جبری “گرما اضافه شده” و “کار انجام شده روی سسیتم” در نظر گرفته شود.
اگر دیواره های محفظه برای ماده و انرژی نفوذ ناپذیر باشند، سیستم مورد نظر یک سیستم منزوی یا ایزوله است که انرژی داخلی آن نمی تواند تغییر کند.
انرژی داخلی حالت خاصی از یک سیستم نمی تواند مستقیما اندازه گیری شود. و معمولا برای ما اهمیت چندانی ندارد که انرژی درونی تک تک مولفه های یک سیستم را بدانیم.
ترمودینامیک عمدتا تنها به تغییرات در انرژی داخلی سیستم اهمیت می دهد و مقدار مطلق مقادیر در ترمودینامیک مهم نیست.
تغییرات یک سیستم نسبت به حالت اولیه ی آن از زنجیره ای از فرآیند های مناسب ترمودینامیکی تشکیل می شود که می توانند حالت مورد نظر نهایی را به وجود آورند. برای آزمایش های عملی در ترمودینامیک و مهندسی، به ندرت لازم است که تمام انرژی های متعلق به هر یک از ذرات یک سیستم را بدست آوریم. از قبیل انرژی که توسط معادله جرم داده شده است. به طور معمول، توصیف ترمودینامیکی فقط موارد مربوط به فرایند های مورد مطالعه را شامل می شود.
انرژی داخلی سیستم یکی از دو تابع حالت اصلی در سیستم است. و مقدار آن فقط به وضعیت نهایی سیستم بستگی دارد و نه به فرآیند هایی که برای ایجاد حالت نهایی آن مورد نیاز بوده است. این مقدار پارامتر بسیار مهمی است و در حقیقت این پارامتر تنها پتانسیل ترمودینامیکی در یک سیستم است زیرا که تمام پتانسیل های ترمودینامیکی دیگر از انرژی داخلی تشکیل شده اند.
در ملاحظات عملی در ترمودینامیک، به ندرت لازم است که تمام انرژی های ذاتی یک سیستم، مانند انرژی که از پایستگی جرم-انرژی ارایه می شود را در نظر بگیریم. به راحتی می توان انرژی درون سیستم را در شرایط میکروسکوپی با استفاده از انرژی جنبشی تصادفی ذرات به علت حرکت میکروسکوپی آن ها در حرکت های انتقالی، چرخشی و ارتعاشی و همچنین با کمک انرژی پتانسیل مرتبط با نیرو های میکروسکوپی، از جمله پیوند های شیمیایی، توضیح داد.
در مکانیک آماری، انرژی داخلی، اثر کلی میانگین مجموع انرژی های جنبشی و پتانسیلی میکروسکوپی سیستم است.
برای مطالعه واکنش های وابسته به درجه حرارت هسته ای اتم ها، انرژی استاتیک ذرات ساکن درون سیستم نیز مهم اند.
واحد انرژی در سیستم بین المللی واحد ها (SI) ژول (J) است. گاهی اوقات راحتتر است که از یک چگالی انرژی متناظر، به نام انرژی داخلی خاصه استفاده کنیم.
این انرژی داخلی خاصه یا نسبت به جرم سیستم، با واحد جرم بر کیلوگرم یا نسبت به مقدار ماده با واحد ژول بر مول، سنجیده می شود.
تاریخچه
جیمز جول رابطه گرما، کار و درجه حرارت را بررسی کرد. او مشاهده کرد که اگر او کار مکانیکی بر روی یک سیال، مانند آب انجام دهد، درجه حرارت آن افزایش می یابد. وی بیان کرد که کار مکانیکی که او بر روی سیستم انجام می داده است به انرژی حرارتی تبدیل می شود.
به طور مشخص، وی دریافت که انرژی به مقدار ۴۱۸۵٫۵ ژول لازم است تا دمای یک کیلوگرم آب، یک درجه سانتی گراد افزایش یابد.
شرح و تعاریف
انرژی داخلی یک سیستم مشخص که با نماد U نمایش داده می شود در مقایسه با حالت استاندارد سیستم، به وسیله ی مجموع انرژی های ماکروسکوپیک انتقال یافته به سیستم اندازه گیری می شود. به سبب همین انرژی های ماکروسکوپیک، سیستم از حالت مرجع به حالت نهایی تبدیل می شود.
انرژی داخلی در یک سیستم، انرژی های ناشی از حرکت یا مکان یک سیستم را شامل نمی شود. بدین معنی که هیچ انرژی جنبشی یا پتانسلی که جسم ممکن است به دلیل حرکت یا موقعیت آن در میدان های گرانشی، الکترواستاتیکی یا الکترومغناطیسی به دست آورده باشد را در این انرژی حساب نمی کنیم.
با این وجود، سهم چنین میدان هایی که سیستم در آن ها قرار گرفته است را به دلیل ایجاد درجات آزادی برای سیستم در نظر می گیریم. در چنین مواردی، میدان در توضیح ترمودینامیکی جسم در قالب یک پارامتر خارجی اضافی گنجانده می شود.