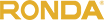- تماس با ما
- 09121001976
- parspalma@gmail.com

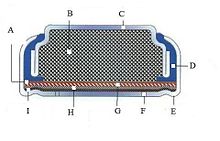
سلول سیلندری
۱۳۹۸-۰۲-۰۷
باتری خودرو های الکتریکی
۱۳۹۸-۰۲-۰۷باتری اکسید روی
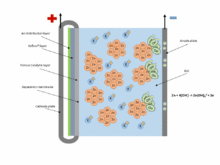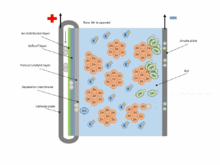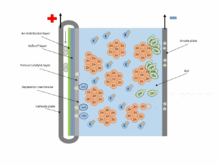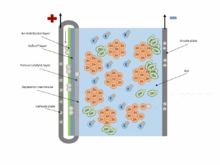
باتری اکسید روی (غیر قابل شارژ) و سلول های سوختی اکسید روی (از لحاظ مکانیکی قابل شارژ) باتری های اکسید متالی هستند که توسط اکسید شدن روی با اکسیژن هوا نیرو می گیرند.
این باتری ها دارای تراکم انرژی بالا و نسبتا ارزان برای تولید هستند.
اندازه هایشان از سلول های دکمه ای بسیار کوچک برای سمعک ها، باتری های بزرگتر در دوربین های فیلمبرداری که قبلا از باتری های جیوه ای در آن ها استفاده می شد، تا باتری های بسیار بزرگ که در وسایل نقلیه الکتریکی استفاده می شود.
باتری های اکسید روی دارای برخی ویژگی های سلول ها و همچنین باتری های سوختی هستند: روی،سوخت است ، سرعت واکنش را می توان با تغییر جریان هوا کنترل کرد، و خمیر و مخلوط روی-الکترولیت اکسید شده میتواند با خمیر تازه ای جایگزین شود.
باتری های روی باتری را می توان در حال حاضر جایگزین باتری های جیوه ای ۱٫۳۵ وات متوقف شده شوند (اگر چه با طول عمر کمتر)، که در دهه های ۱۹۷۰ تا ۱۹۸۰ معمولا در دوربین های عکاسی استفاده می شدند.
کاربرد های آینده این باتری عبارتند از: گسترش آن به عنوان یک باتری الکتریکی خودرو و به عنوان یک سیستم ذخیره انرژی در مقیاس کاربردی.
تاریخچه
اثر اکسیژن در اوایل قرن ۱۹ شناخته شد، زمانی که باتری های مرطوب Leclanche ، اکسیژن اتمسفر را در جمع کننده جریان کاتد کربن جذب کرد.
سلول های اولیه بزرگ اکسید روی از قبیل نوع Carbonaire صنایع Thomas A. Edisonهستند که در علامت دهی راه آهن،سایت های ارتباط از راه دور و شناور های ناوبری استفاده می شده اند.این ها کاربرد هایی طولانی مدت و کم هزینه بودند.
توسعه الکترود های نازک مبتنی بر تحقیق سلول سوختی در دهه ۱۹۷۰ میلادی، امکان استفاده از سلول های دکمه ای کوچک و سلول های اصلی منشوری برای سمک ها، پیجر ها، و تجهیزات پزشکی، به ویژه تله متر قلب را فراهم کرد.
اولین باتری قابل شارژ اکسید روی در سال ۱۹۹۶ توسط یک نوآور اسلوونیایی، Miro Zoric ساخته شد.
اولین وسایل نقلیه در جاده ها که از باتری های اکسید روی استفاده می کردند، اتوبوس های کوچک و متوسط در سنگاپور بود، جایی که Zoric برنامه انتقال برق ملی را در پلی تکنیک سنگاپور در طی پست انتقال تکنولوژی خود رهبری می کرد.
خط مونتاژ تولید انبوه برای باتری های اکسید روی او در سال ۱۹۹۷ راه اندازی شد.
این سلول ها تراکم انرژی بالاتر و ضریب انرژی ( و وزن) خاصی را در مقایسه با باتری های اسید سرب استاندارد آن زمان ارائه می دادند.
تراکم ذخیره سازی
باتری های اکسید روی دارای تراکم انرژی بیشتر و نسبت انرژی (و وزن) خاصی نسبت به سایر انواع باتری ها هستند زیرا اتمسفر هوا یکی از واکنش های باتری است. هوا با باتری بسته بندی نمی شود، به طوری که یک سلول می تواند روی درون آند بیشتری از یک سلول استفاده کند که باید شامل مثلا دی اکسید منگنز نیز باشد. این، ظرفیت را برای وزن یا حجم مشخص افزایش می دهد. به عنوان مثال یک باتری اکسید روی با قطر ۱۱٫۶ میلیمتر و ارتفاع ۵٫۴ میلیمتر از یک تولید کننده دارای ظرفیت ۶۲۰ میلی آمپر و وزن ۱٫۹ گرم است. سلول های اکسید سیلور مختلف (SR44) و سلول های آلکالاین با اندازه ی مشابه، ۱۵۰-۲۰۰ میلی آمپر و وزن ۲٫۳-۲٫۴ گرم را تامین می کنند.
ذخیره سازی و عمر عملیاتی
سلول های اکسید روی دارای طول عمر طولانی هستند اگر برای بیرون نگه داشتن هوا خوب مهر و موم شده باشند؛ حتی سلول های دکمه ای کوچک می توانند تا ۳ سال در دمای اتاق با کمی کاهش ظرفیت نگهداری شوند، اگر مهر و موم آن ها برداشته نشود. سلول های صنعتی ذخیره شده در حالت خشک دارای عمر ذخیره سازی نامحدود هستند.
انواع سلول
اولیه (غیر قابل شارژ)
باتری های اکسید روی بزرگ، با ظرفیت تا ۲۰۰۰ آمپر ساعت در هر سلول برای نیرو دادن به ابزارهای ناوبری و چراغ های نشانگر، آزمایش های اقیانوس شناسی و سیگنال های راه آهن مورد استفاده قرار می گیرند.
ثانویه (قابل شارژ)
سلول های اکسید روی قابل شارژ نیاز به ته نشینی روی از الکترولیتِ بر پایه آب دارد تا بطور نزدیک قابل کنترل باشد. چالش ها شامل تشکیل دندریت، انحلال غیر یکنواخت روی و حلالیت محدود در الکترولیت ها است.
شارژ مکانیکی
سیستم های قابل شارژ می توانند از نظر مکانیکی آند و الکترولیت را جایگزین کنند، که اساسا به عنوان یک سلول اولیه قابل تعمیر عمل می کنند، یا می توانند از پودر روی یا سایر روش ها برای دوباره پر کردن واکنش دهنده استفاده کنند.
سیستم های شارژ مکانیکی برای استفاده در تجهیزات نظامی در دهه ۱۹۶۰ بعلت تراکم انرژی بالا و شارژ آسان مورد بررسی قرار گرفت.
مواد
کاتالیزورها
کاتالیزور کاهش اکسیژن هیبرید نانو لوله کربن / اکسید کبالت و کاتالیزور های کاتدی تکاملی اکسیژن هیدروکسید دو لایه نیکل-آهن، فعالیت کاتالیستی و دوام بیشتری را در الکترولیت آلکالاین متمرکز نسبت به کاتالیزورهای ارزشمند پلاتینیوم متال و ایریدیم دارند.