- تماس با ما
- 09121001976
- parspalma@gmail.com
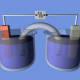
سلول الکتروشیمیایی
۱۳۹۸-۰۱-۰۳
باتری نیکل-متال هیدرید
۱۳۹۸-۰۱-۰۳باتری لیتیوم پلیمر
یک باتری لیتیوم پلیمر یا به اصطلاح باتری لیتیوم یون پلیمر (به اختصار LiPo، LIP، Li-poly، لیتیوم پلی و غیره) یک باتری قابل شارژ از فناوری یون لیتیوم با استفاده از یک الکترولیت پلیمری به جای یک الکترولیت مایع است. پلیمرهای نیمه جامد (ژل) رسانایی بالا این الکترولیت را تشکیل می دهند. این باتری انرژی خاصی را نسبت به سایر انواع باتری لیتیوم ارائه می دهد و در برنامه های کاربردی استفاده می شود که وزن آن یک ویژگی حیاتی است مانند دستگاه های تلفن همراه و هواپیماهای رادیویی.

تاریخچه
سلول های LiPo با دنبال کردن سلول های لیتیوم یون و لیتیوم فلزی که طی دهه ۱۹۸۰ تحت تحقیق گسترده ای قرار گرفته اند، به مرحله ی مهمی از اولین سلول لیتیوم یونی تجاری تجاری سونی در سال ۱۹۹۱ رسید. پس از آن، دیگر فرم های بسته بندی تکامل یافتند، از جمله قالب کیسه ای که در حال حاضر نیز به نام Lipo نامیده می شوند.
مبانی طراحی و اصطلاحات
سلول های پلیمری لیتیوم از باتری های لیتیوم یون و لیتیوم فلزی تشکیل شده است. تفاوت اصلی استفاده از یک الکترولیت لیتیوم نمک مایع (مانند لیپوف ۶) در حلال آلی باتری از الکترولیت پلیمر جامد مانند پلی اتیلن اکسید ،پلی (اکریلنیتیل) ، پلی متیل متاکریلات یا پلی (وینیلیدین فلوراید) است.
الکترولیت جامد به طور معمول می تواند به عنوان یکی از سه نوع طبقه بندی شود: SPE خشک، SPE ژله ای و SPE متخلخل. SPE خشک برای اولین بار در باتری های نمونه مورد استفاده قرار گرفت. از سال ۱۹۹۰، سازمان های متعددی نظیر Mead و Valence در ایالات متحده و GS Yuasa در ژاپن باتری هایی با استفاده از SPE های ژل را توسعه دادند. در سال ۱۹۹۶، Bellcore در ایالات متحده یک لایه پلیمری قابل شارژ با استفاده از SPE متخلخل اعلام کرد.
یک سلول معمولی دارای چهار جزء اصلی است: الکترود مثبت، الکترود منفی، جداساز و الکترولیت. خود جداساز ممکن است یک پلیمر باشد، مانند یک فیلم کوچک از پلی اتیلن بنابراین، حتی زمانی که سلول دارای الکترولیت مایع است، آن را هنوز هم دارای جزیی از پلیمر می دانند. علاوه بر این، الکترود مثبت را می توان به سه بخش تقسیم کرد: لیتیوم انتقال فلز اکسید (مانند LiCoO2 یا LiMn2O4)، یک افزودنی رسانا و یک پیوند پلیمری از پلی (وینیلیدین فلوراید). الکترود منفی مواد ممکن است همان سه بخش را داشته باشد، فقط کربن جایگزین فلز لیتیوم-اکسید می شود.
کارکرد اساسی
همانند دیگر سلولهای یون لیتیوم، LiPo ها بر روی اصل تداخل و انحراف یونهای لیتیوم از یک ماده الکترود مثبت و منفی کار می کنند ،در حالیکه الکترولیت مایع یک ماده هدایت کننده ایجاد می کند.
برای جلوگیری از تماس مستقیم الکترودها با یکدیگر، جداسازی میکروپروس مورد بحث قرار می گیرد تا تنها یون ها و نه ذرات الکترود جا به جا شوند.
روش شارژ
ولتاژ یک سلول لیپو به شیمی آن بستگی دارد و از حدود ۲٫۷-۳٫۰ V (تخلیه شده) تا حدود ۴٫۲ V (کاملا شارژ) متفاوت است، برای سلول های مبتنی بر اسیدهای لیتیوم فلز (مانند LiCoO2) و حدود ۱٫۸-۲٫۰ V (تخلیه شده) به ۳٫۶-۳٫۸ V (شارژ) و برای سلول های مبتنی بر لیتیوم آهن فسفات (LiFePO4). همین مقدار می باشد.
برای بسته باتری های لیپو با با سلول های متصل به سری، یک شارژر تخصصی می تواند شارژ را بر اساس هر سلولی نظارت کند، به طوری که تمام سلول ها به همان وضعیت شارژ (SOC) آورده شوند.
ایمنی
سلول های LiPo با مشکلات مشابه با سایر سلول های یون لیتیوم مواجه هستند. این به این معنی است که شارژ بیش از حد،تخلیه بی اساس، دمای بالا، اتصال کوتاه، نفوذ و خرد شدن ممکن است به یک شکست فاجعه بار، از جمله خراب شدن کیسه، نشت الکترولیت و آتش سوزی منجر شوند.
تمام سلولهای لیتیوم در سطح بالاتر شارژ یا شارژ بیش از اندازه به علت تبخیر ناشی از الکترولیت گسترش می یابند.

اعمال فشار بر روی سلول های LiPo
بر خلاف سلول های استوانه ای و منشوری لیتیوم یونی که دارای یک مورد فلزی سفت و سخت هستند، سلول های LiPo دارای یک لایه انعطاف پذیر (فوم پلیمری) هستند، به طوری که نسبتا محدودیتی ندارند. خود این سلول ها بیش از ۲۰٪ سبک تر از سلول های استوانه ای معادل همان ظرفیت هستند.
داشتن وزن سبک، مزیت محسوب می شود همانگونه که هنگام استفاده از هواپیمای راه دور به وزن سبک آن کمک می کند. با این حال، مشخص شده است که فشار متوسط روی لایه هایی که سلول را تشکیل می دهند، باعث افزایش ظرفیت نگهداری می شود زیرا ارتباط بین اجزاء به حداکثر می رسد و منجر به تغییر همراه با افزایش مقاومت ظاهری و در نهایت تخریب همراه می شوند.

موارد استفاده
سلول های LiPo به تولید کنندگان برتری های خود را می نمایانند. آنها به راحتی می توانند باتری هایی تقریبا با هر شکل ظاهری را تولید کنند. به عنوان مثال،برای نیازهای فضا و وزن دستگاه های تلفن همراه و نوت بوک ها می تواند کاملا رضایت بخش باشد. همچنین، آنها میزان تخلیه کمی دارند، که در حدود ۵٪ در هر ماه است.