- تماس با ما
- 09121001976
- parspalma@gmail.com

باتری های لیتیوم
۱۳۹۷-۱۲-۲۹
باتری لیتیوم پلیمر
۱۳۹۷-۱۲-۲۹سلول الکتروشیمیایی
یک سلول الکتروشیمیایی دستگاهی است که قادر به تولید انرژی الکتریکی از واکنش های شیمیایی یا استفاده از انرژی الکتریکی برای ایجاد واکنش های شیمیایی است. سلولهای الکتروشیمیایی که جریان الکتریسیته تولید می کنند، سلول های ولتائیک یا سلول های گالوانیکی نامیده می شوند و آنانی که به طور مثال از طریق الکترولیز واکنش های شیمیایی را تولید می کنند، سلول های الکترولیتی نامیده می شوند. مثال معمولی از یک سلول گالوانیکی، یک سلول ۱٫۵ ولت استاندارد است که برای مصرف مورد استفاده قرار می گیرد. یک باتری شامل یک یا چند سلول است که به صورت موازی، سری یا سری و موازی متصل می شوند.
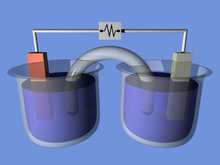
سلول الکترولیتیک
یک سلول الکترولیتیکی یک سلول الکتروشیمیایی است که از طریق استفاده از انرژی الکتریکی یک واکنش غیر واگیر را مجدد انجام می دهد. نمونه های مهم الکترولیز تجزیه آب به هیدروژن و اکسیژن و بوکسیت به آلومینیوم و سایر مواد شیمیایی است. الکترولیز کردن (به عنوان مثال از مس، نقره، نیکل یا کروم) با استفاده از یک سلول الکترولیتی انجام می شود. الکترولیز یک تکنیک است که از جریان الکتریکی مستقیم استفاده می کند.
یک سلول الکترولیتی دارای سه جزء است: الکترولیت و دو الکترود (یک کاتد و یک آند). الکترولیت معمولا محلول آب یا سایر حلالها است که در آن یونها حل شده اند. نمک های مذاب مانند کلرید سدیم نیز الکترولیت هستند. هنگامی که توسط ولتاژ خارجی اعمال شده به الکترودها هدایت می شود، یون های الکترولیت به یک الکترود با شار مخالفت جذب می شوند، جایی که واکنش های انتقال بار (همچنین به نام فارادائیک یا ردوکس) می توانند انجام شوند. تنها با یک پتانسیل الکتریکی خارجی (یعنی ولتاژ) قطب راست و می توان یک سلول الکترولیتی ترکیب شیمیایی را به طور معمول پایدار یا بی اثر در محلول تجزیه کرد. انرژی الکتریکی ارائه شده می تواند یک واکنش شیمیایی ایجاد کند که در غیر این صورت خود به خود رخ نمی دهد.
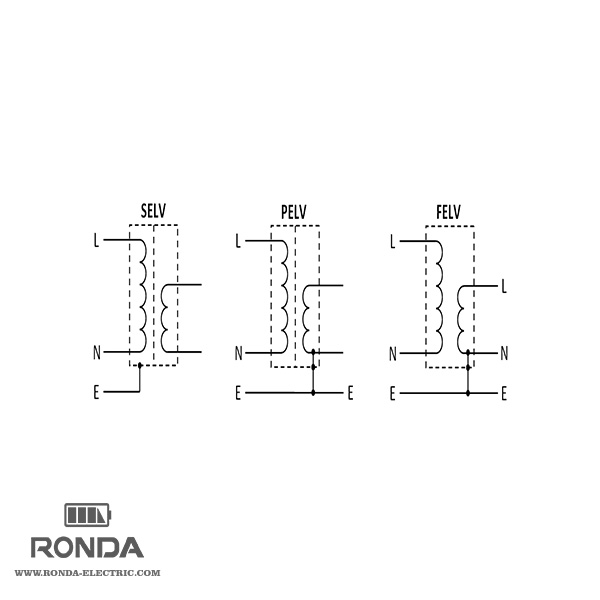
سلول گالوانیک یا سلول ولتائیک
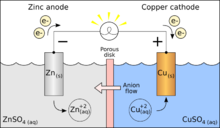
سلول گالوانیکی یا سلولهای ولتائیک که به ترتیب به نام لوئیجی گالوانی یا الساندرو والنته نامگذاری شده است، یک سلول الکتروشیمیایی است که انرژی الکتریکی را از واکنش های خود به خود درون سلول ایجاد می کند.به طور کلی متشکل از دو فلز مختلف متصل به یک پل نمکی یا نیمه سلولی فردی است که توسط غشای متخلخل جدا شده اند.
ولتا مخترع پیل ولتائیک، اولین باتری الکتریکی بود. در استفاده معمول، کلمه “battery” آمده است که شامل یک سلول گالوانیزه تک، اما یک باتری به درستی از سلول های چندگانه تشکیل شده است.
سلول اولیه
یک سلول اولیه یک باتری گالوانیک است که برای یکبار استفاده و دور انداخته می شود و با برق مجددا شارژ نشده و مانند یک سلول ثانویه (باتری قابل شارژ) مجددا استفاده می شود. به طور کلی، واکنش الکتروشیمیایی که در سلول اتفاق می افتد، برگشت پذیر نیست، و این باعث می شود که سلول غیر قابل شارژ شود. یک سلول اولیه زمانی که استفاده می شود، واکنش های شیمیایی در باتری از مواد شیمیایی تولید کننده انرژی استفاده می کنند؛ هنگامی که آنها رو به اتمام روند، باتری تولید برق را متوقف می کند و بی فایده است. در مقابل، در یک سلول ثانویه، واکنش را می توان با جریان دادن به سلول با یک شارژر باتری برای شارژ آن، احیاء واکنش دهنده های شیمیایی، معکوس کرد. سلولهای اولیه در گستره ای از اندازه های استاندارد ساخته شده اند تا لوازم خانگی کوچک مانند چراغ قوه و رادیوهای قابل حمل را قدرت دهند.
باتری اولیه حدود ۹۰ درصد از بازار باتری ۵۰ میلیارد دلاری را تشکیل می دهد، اما باتری های ثانویه سهم بازار را به دست آورده اند. حدود ۱۵ میلیارد باتری اولیه در هر سال در سراسر جهان به دور انداخته می شوند.با توجه به فلزات سنگین سمی و اسیدهای قوی یا قلیایی که در آنها وجود دارد، باتری ها زباله های خطرناکی هستند. اکثر شهرداری ها آنها را طبقه بندی می کنند و نیاز به دفع جداگانه دارند. انرژی مورد نیاز برای تولید باتری حدود ۵۰ برابر انرژی موجود در آن است. با توجه به محتوای آلاینده بالا آنها در مقایسه با محتوای انرژی کم آنها، باتری اولیه، فناوری ناسازگار و غیرمستقیم محیطی محسوب می شود. با توجه به افزایش فروش دستگاه های بی سیم و ابزارهای بی سیم که نمی توانند از لحاظ اقتصادی از باتری های اصلی تامین شوند و با باتری های قابل شارژ مجزا عرضه شوند، صنعت باتری ثانویه دارای رشد بالا است و به سختی جایگزین باتری اصلی در محصولات با کیفیت بالا شده است.
سلول ثانویه
یک سلول ثانویه، معمولا به عنوان یک باتری قابل شارژ شناخته می شود، یک سلول الکتروشیمیایی می تواند به عنوان یک سلول گالوانیکی یا به عنوان یک سلول الکترولیتی نیز عمل کند. این به عنوان یک راه مناسب برای ذخیره برق استفاده می شود، زمانی که جریان افزایش می یابد، سطوح یک یا چند مواد شیمیایی را تشکیل می دهد (شارژ) و در حالی که تخلیه آنها کاهش می یابد و نیروی الکتروموتور حاصل می تواند به خوبی عمل کند.